L’équipe F16, riche de ses compétences multidisciplinaires transversales et complémentaires en chimie, physicochimie et biologie poursuit 3 objectifs principaux, avec un très fort positionnement en oncologie :
- Objectif 1 : synthétiser de nouvelles molécules d’intérêt thérapeutique en oncologie et en infectiologie, et comprendre leur mécanisme d’action,
- Objectif 2 : identifier de nouvelles cibles thérapeutiques en oncologie, par l’étude des mécanismes de chimiorésistance tumorale,
- Objectif 3 : développer de nouveaux modèles alternatifs (vitro, vivo et ex-ovo) utilisables en oncopharmacologie, senescence (Nématode, Tardigrade, CAM), et en pharmacotoxicologie cutanée sur l’absorption des xénobiotiques et la formulation des actifs.
Nos Thématiques
Chimie Médicinale / Oncopharmacochimie
Chimie Médicinale / Oncopharmacochimie (Pierre-Antoine BONNET, Carine MASQUEFA, responsables)
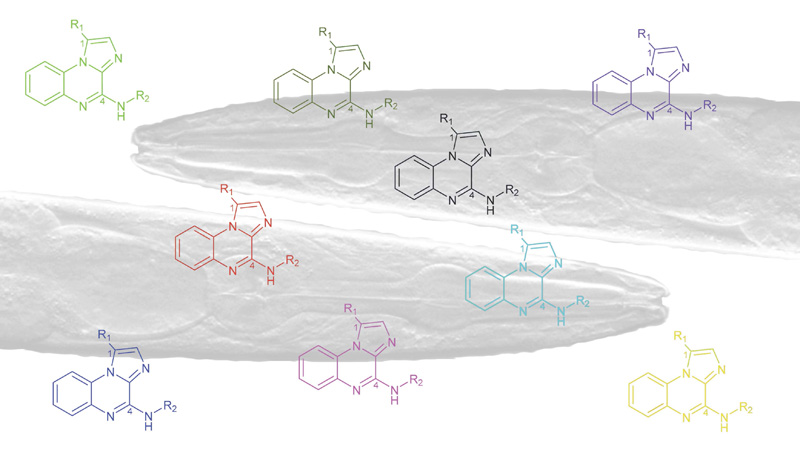
L’équipe se concentre sur le développement de nouveaux composés hétérocycliques dotés d’activités anticancéreuses et immunomodulatrices. Les approches de Chimie Médicinale utilisées pour la série Imiqualines, ses 3 générations de produits et l’amélioration de 3 logs de l’activité cytotoxique sur diverses lignées cellulaires cancéreuses humaines constituent l’essentiel de l’orientation scientifique du Groupe. Cette orientation bénéficie d’un soutien fort et continu de la SaTT AxLR dans le cadre du projet MUSE, de l’IRCM via la plateforme MPCC soutenue par le SIRIC et de plusieurs partenariats internationaux très productifs. D’un point de vue chimique, la diversité pour les prochaines générations d’imiqualines sera obtenue par d’autres modifications et substitutions du principal hétérocycle imidazo[1,2-a]quinoxaline en utilisant des couplages croisés tels que Sonogashira, Suzuki-Miyaura ou Buchwald-Hartwig. des réactions ou autres substitutions nucléophiles classiques sont bien connues au sein de l’équipe : imidazo[1,5-a]quinoxaline et pyrazolo[1,5-a]quinoxaline.
Mécanisme d’action de nouvelles molécules actives
Mécanisme d’action de nouvelles molécules actives (Pierre CUQ, Laure-Anaïs VINCENT, responsables)
Deux projets principaux sont développés : i) le projet « imiqualines », à l’origine de la formation du Team F16 avec le Pr. PA BONNET et Pr. C MASQUÉFA, ii) le projet « diazépinones » en collaboration avec le Pr. N MASURIER (F9-IBMM), avec le soutien du consortium MUSE. Le groupe 2 supervise la partie biologique de la détermination du mécanisme d’action (MOA) et de l’identification des cibles pharmacologiques des nouvelles molécules actives. Cette étape, cruciale dans le développement des candidats médicaments, est réalisée en étroite collaboration avec les Groupes 1 et 3. Ainsi, chaque tâche est pensée de manière transversale et synergique dans un objectif de valorisation. Les nouvelles familles de composés actifs sont dans un premier temps brevetées pour envisager le développement des meilleurs composés à travers des programmes de maturation. Néanmoins, notre objectif majeur reste de publier à moyen terme dans des journaux internationaux à fort impact.
Modèles alternatifs de pharmacotoxicologie appliqués aux produits xénobiotiques et au vieillissement
Modèles alternatifs de pharmacotoxicologie appliqués aux produits xénobiotiques et au vieillissement (Simon GALAS resonsable)
Cette équipe rassemble des modèles alternatifs dédiés à de nouveaux modèles expérimentaux afin d’évaluer les propriétés de molécules actives telles que les molécules transdermiques perméables, les molécules cytotoxiques sur les biopsies humaines ainsi que l’effet multigénérationnel aigu et chronique de molécules agissant sur le stress cellulaire et la capacité de prolifération, y compris les chimiorésistances acquises. Nous développons davantage le modèle Caenorhabditis et la boîte à outils de génétique moléculaire qui l’accompagne afin d’évaluer l’effet in vivo de nouvelles molécules dirigées contre la chimiorésistance acquise ainsi que leur impact à l’échelle multigénérationnelle et sur la résistance au stress et le processus de vieillissement. Nous évaluons également les éventuels effets hormétiques et épigénétiques des molécules. Notre expertise permet également de réaliser de nouvelles évaluations de la toxicité des gaz vers des collaborations industrielles. Nous développons également un nouveau modèle in vivo : le tardigrade, considéré comme l’un des organismes les plus résistants au monde. Nous avons l’intention de développer une boîte à outils de génétique moléculaire pour ce modèle émergent afin d’évaluer l’activité des molécules et les cibles biologiques.


